03 March 2021
La terapia antibiótica ha sido crucial para controlar enfermedades infecciosas y mejorar así el bienestar animal y la salud del consumidor final, siendo considerada, junto con las vacunas, los avances científicos que han salvado más vidas en la historia de la humanidad.
Sin embargo, la aparición y creciente evolución de las resistencias de las bacterias a los antibióticos –resistencias antimicrobianas– ha implicado la limitación del uso de antibióticos, tanto por una menor efectividad como por una mayor restricción legal.
Así, y en el marco de One Health –la salud humana y la sanidad animal son interdependientes y están vinculadas a los ecosistemas en los cuales coexisten–, la búsqueda de alternativas para controlar las poblaciones bacterianas es un reto clave al que se enfrenta la sanidad animal y la medicina humana del siglo XXI.
Una alternativa cada vez más estudiada es la terapia fágica o fagoterapia. A pesar no ser una alternativa novedosa –se descubrió con anterioridad a la terapia antibiótica– quedó marginada gracias al éxito de la antibioterapia.
¿Qué son los fagos?
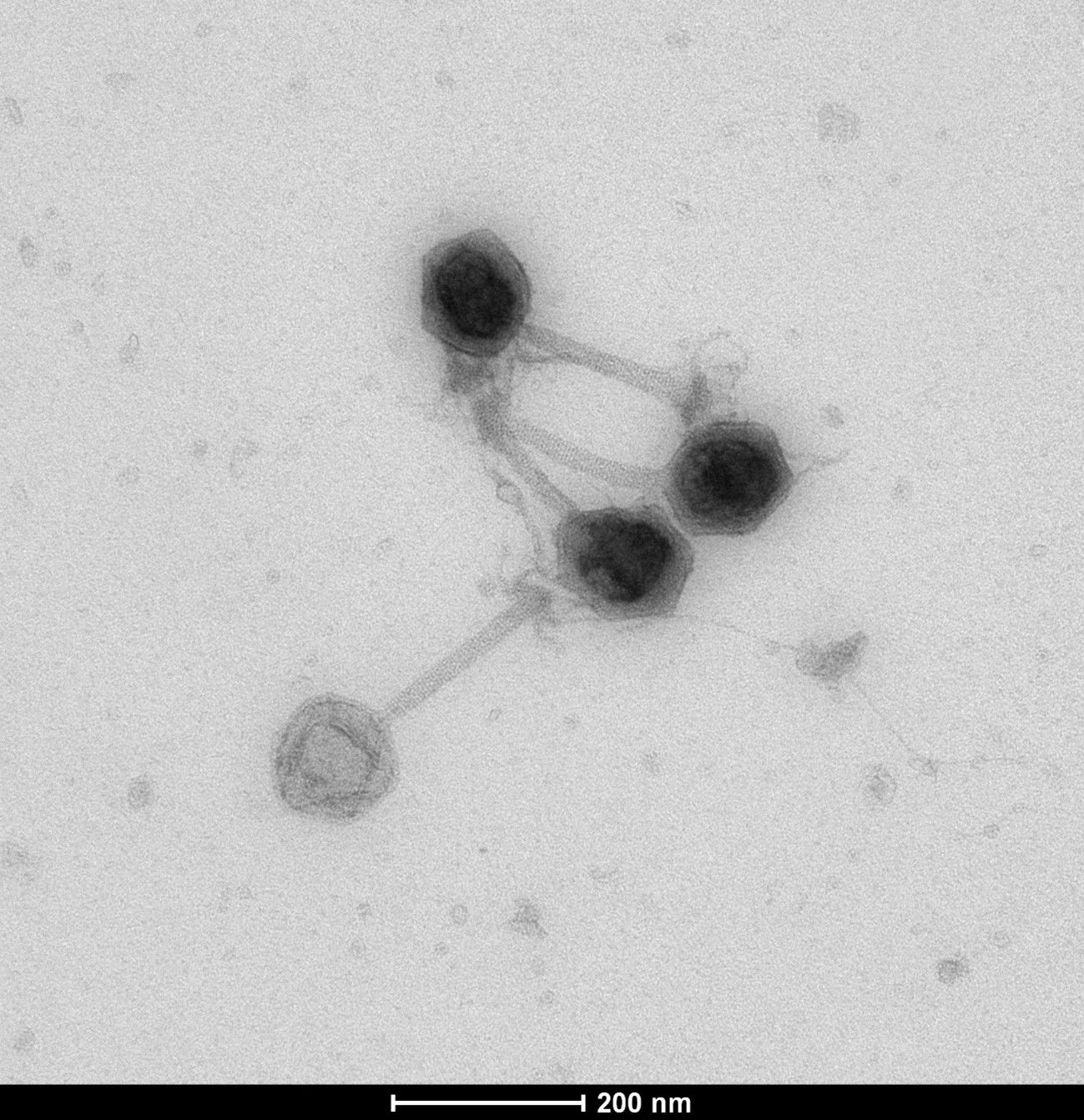
Los bacteriófagos –o fagos– son los microorganismos más abundantes en la naturaleza. Se conocen miles de ellos, y cada año se describen cientos nuevos, esto hace de los bacteriófagos el más amplio grupo de virus conocido. El 96% de los bacteriófagos conocidos pertenecen a 3 familias:
- Myoviridae
- Podoviridae
- Siphoviridae
Todas ellas pertenecientes al orden de los Caudovirales, virus con cola.
La terapia antibiótica junto con las vacunas son los avances científicos que han salvado más vidas en la historia de la humanidad
¿Por qué los fagos pueden ser útiles para controlar enfermedades?
El potencial uso de los fagos para el tratamiento de enfermedades infecciosas se describió por el francocanadiense Félix d´Hérelle en 1917, durante sus investigaciones sobre disentería en soldados franceses de la I Guerra Mundial, cuando el término “bacteriófago” fue presentado por él en el Instituto Pasteur de Paris. Así, desde su descubrimiento a principios del siglo XX, se han venido empleando en la medicina humana para tratar infecciones.
Sin embargo, el uso efectivo y generalizado de los antibióticos tras la II Guerra Mundial, junto con las dificultades tecnológicas de estandarización para demostrar resultados concluyentes y el desconocimiento de su biología y farmacodinámica, condujeron al abandono de la fagoterapia, con la excepción algunos países de Europa Oriental y en la antigua Unión Soviética.
Los fagos se encuentran en simbiosis con las bacterias, su organismo diana. Están presentes ubiquitariamente en el medioambiente que nos rodea, solo tienen receptores para las células procariotas y una vez no tienen bacterias en las que replicarse, reducen su número hasta su estado inicial.
- Son naturales –los encontramos en el ecosistema
- Específicos –a diferencia de los antibióticos, atacarán solo a aquellas bacterias diana frente a las que dirijamos la terapia sin afectar al resto de la microbiota
- Autolimitantes –son de replicación autolimitante y eliminan su acción cuando no queda bacteria huésped
- Antibiorresistencias-independientes –los mecanismos de resistencias antimicrobianas son independientes de los mecanismos de resistencias fágicas
- Y tienen propiedades anti-biofilm
Estas características hacen de ellos unos candidatos interesantes para el control de las poblaciones bacterianas en una suerte de lucha biológica.
¿Cómo se emplean los fagos?
La aplicación de cócteles de bacteriófagos –mezcla de varios fagos– es la vía comúnmente empleada para su uso en alimentos, superficies, animales y humanos.
- En primer lugar debemos aislar y caracterizar la bacteria frente a la cual queremos dirigir la terapia.
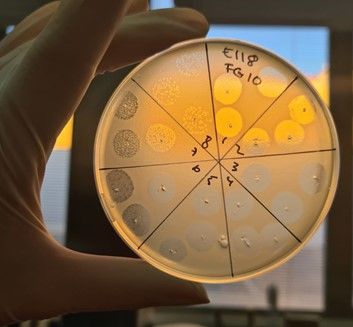
- Posteriormente, a partir de una fagoteca o mediante nuevo aislamiento del ecosistema, se seleccionan los fagos activos frente al patógeno mediante la realización de un fagograma –el equivalente de un antibiograma, empleando fagos en vez de antibióticos.
- Por último, se multiplican –escalado–, se combinan y se administran.
En este sentido, en el año 2018 introdujimos un nuevo concepto, el autobacteriófago o autofago. Se trata de un bacteriófago aislado directamente del mismo medio donde se encuentra la bacteria diana. El objetivo esobtener una combinación muy específica, sin introducir fagos externos en el ecosistema en concreto. Esta estrategia podría aquí asimilarse al de las autovacunas.
La vía de aplicación dependerá de la ubicación de las bacterias diana, podemos encontrar desde aplicaciones en superficies de instalaciones –biocida–, alimentos, tópica, oral, parenteral o incluso vía aerosol.
¿Qué ejemplos existen de terapia fágica?
Existen numerosas áreas de actuación de la terapia fágica, que podemos agrupar en medicina humana, seguridad alimentaria, sanidad animal y vegetal.
Los bacteriófagos se emplean actualmente como terapia antibacteriana rutinaria en los países del antiguo bloque soviético, como Rusia, Polonia o Georgia, ya que estos países nunca abandonaron el estudio de los bacteriófagos como terapia antimicrobiana.

Además, en USA ya se comercializan como desinfectantes en industria alimentaria contra Salmonella, Escherichiacoliy Listeriamonocytogenes. Por lo que respecta a Europa, existen empresas que han iniciado la carrera europea de la producción y comercialización de preparados fágicos, como la holandesa MICREOS o la alemana FINKTEC.
Además, en el caso de la ganadería –sanidad animal y seguridad alimentaria–, existe numerosas publicaciones reportando resultados esperanzadores frente a bacterias como Salmonella o E.coli, tanto a nivel experimental como comercial.
Por ejemplo, en el siguiente trabajo “Salmonella Infantis and Salmonella Enteritidis specific bacteriophages isolated form poultry faeces as a complementary tool for cleaning and disinfection against Salmonella” publicado en la revista Comparative Immunology, Microbiology and Infectious Diseases (Volumen 68,febrero de 2020) por nuestro grupo, destacamos lo siguientes resultados:
Se obtuvo como resultado óptimo una reducción de 4,55 log de Salmonella Infantis en el suelo de una nave experimental avícola contaminada con 108 UFC/mL tras 2 aplicaciones consecutivas de bacteriófago a una concentración de 108 UFP/mL.
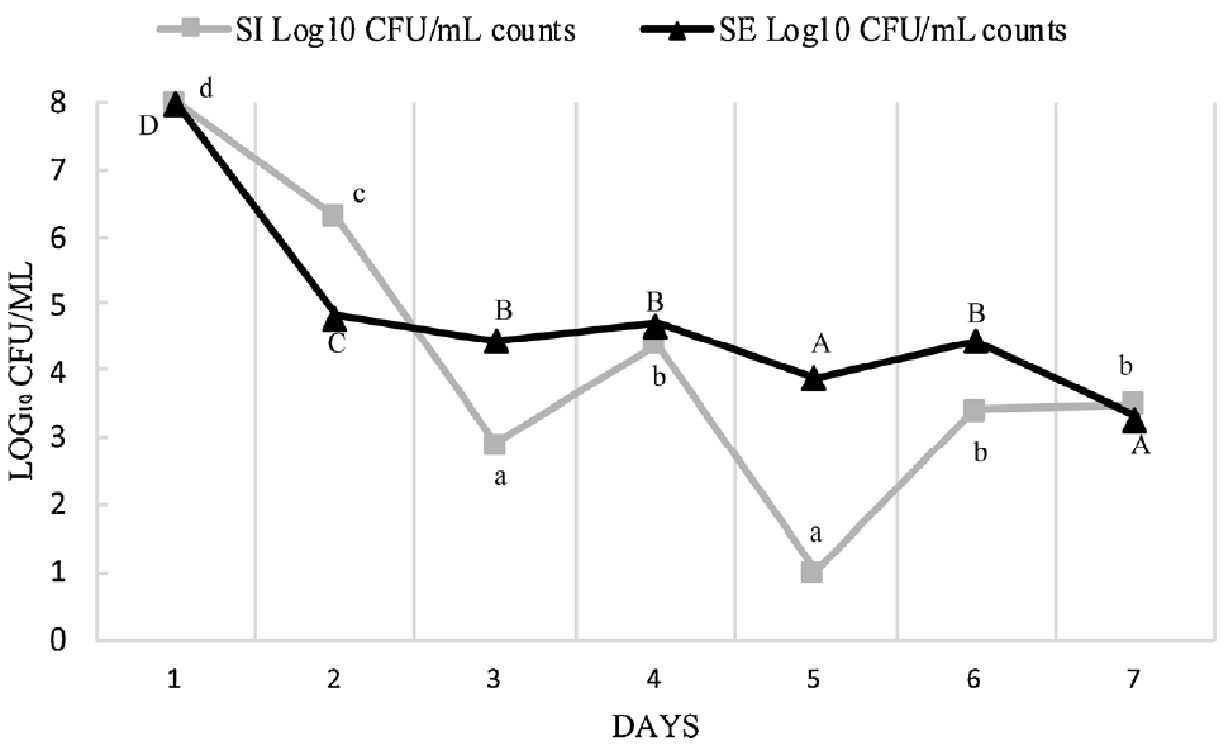
Por otro lado, en la siguiente figura, se muestra la reducción de Salmonella Infantis y Salmonella Enteritidis a lo largo de la semana (7 días), tras la aplicación consecutiva de dos dosis de autofago a una concentración de 108 UFCP/mL y 103 UFP/mL. Los resultados muestran una reducción de 7 log CFU/mL y 4,1 log CFU/mL de SalmonellaInfantis (SI) y Salmonella Enteritidis (SE) el 5º día tras la aplicación de los autofagos.
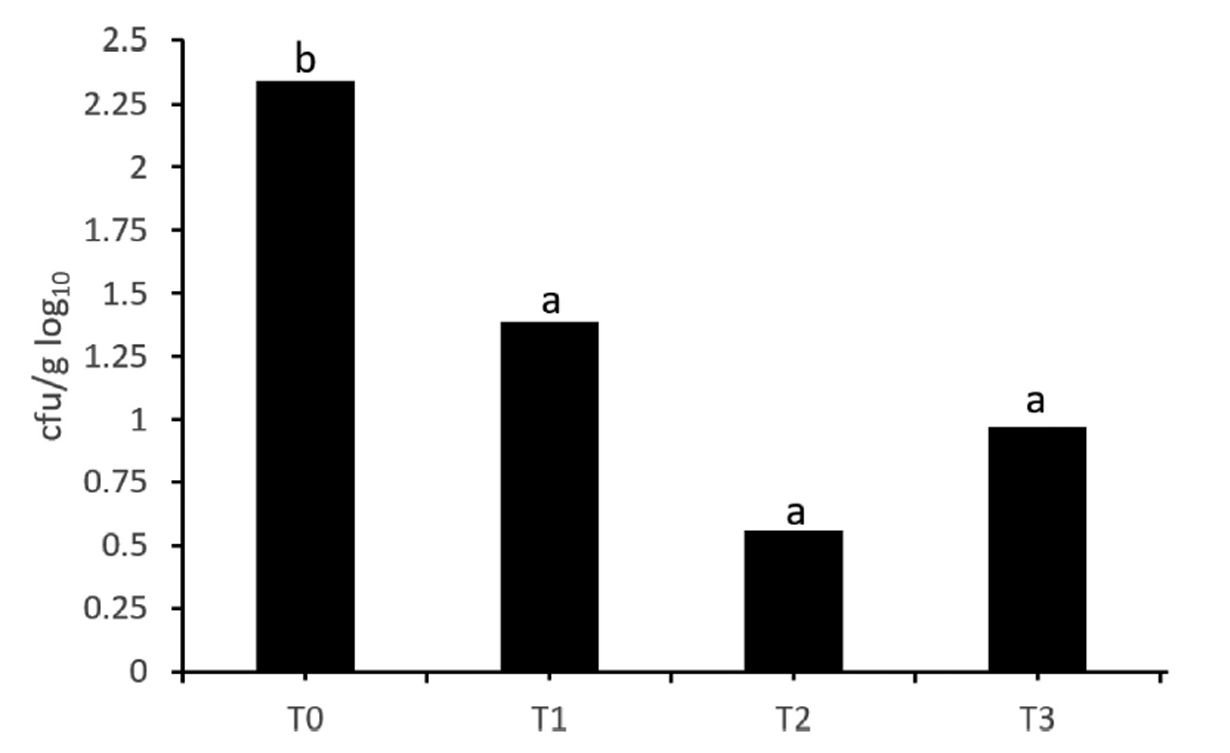
En este otro estudio, “Autophage as a control measure for Salmonella in laying hens”, publicado por nuestro equipo en diciembre de 2018 en la revista Poultry Science (Volumen 97), realizado en condiciones experimentales en una granja comercial positiva a Salmonella Enteritidis, se obtuvo resultado de ausencia de Salmonella en muestras tomadas de superficies tras 2 aplicaciones consecutivas de autofagos, separadas en intervalos de 24h. Por lo que respecta a las muestras de heces de los animales, se obtuvo una reducción significativa de la concentración de Salmonella entre las muestras tomadas antes y después de la aplicación del autofago.

En este sentido, la Comisión Europea ha cofinanciado varios proyectos de investigación relacionados con la terapia fágica, como pueden ser PHAGOVET y C-SNIPER en avicultura, AQUAPHAGE en acuicultura, VIROPLANT en vegetales, PhagoPROD, CUREy AntibioPhage en medicina humana.
¿Cuáles son los retos a los que se enfrenta la terapia fágica?
Desde la caracterización de los fagos hasta su desarrollo clínico y aplicación en campo, existen escollos técnicos y regulatorios.
En cuanto a los retos técnicos, podemos nombrar la ampliación de los procesos de fabricación para contar con plantas de escalado que permitan grandes producciones, la limitada acción intracelular, la liberación de endotoxinas tras la lisis celular, la interacción con el sistema inmune o la existencia de resistencias, la aceptación social, la prevención del uso de virus de ciclos lisogénicos y la transmisión de genes de antibiorresistencia o virulencia.
¿Qué futuro espera a la terapia fágica?
En cuanto al aspecto regulatorio en la UE, se espera contar con un marco favorable en los próximos años, contando, de momento, con una opinión favorable de la EFSA para el uso en alimentos.
Los bacteriófagos han surgido como una solución prometedora al desafío global de los patógenos resistentes a los antimicrobianos, así como una serie de otras patologías relacionadas con la disbiosis del microbioma.
Los progresos técnicos están siendo acompañados de aspectos comerciales, como la cotización cercana a los 100 millones de dólares de BiomX Inc, el acuerdo de Locus Biosciences con BARDA a finales de 2020 para adelantar un programa de 144 millones de dólares para desarrollar un producto a base de bacteriófagos, y con CARB-X por valor de 14 millones de dólares para combatir infecciones por Klebsiellapneumoniae.
Más recientemente, en enero de 2021, se produjo la asociación entre Eligo Biosciences y GSK, valorada en 224 millones de dólares, para combatir el acné mediante un tratamiento pionero que utiliza partículas derivadas de fagos para administrar una nucleasa CRISPR-Cas en ciertas poblaciones bacterianas implicadas.

