
29 December 2020
Introducción: la bioeconomía como único futuro
La bioeconomía, según define la Organización para la Cooperación y el Desarrollo Económicos (OCDE), comprende la aplicación del conocimiento biotecnológico en la potenciación de la producción primaria, la salud y la industria. La bioeconomía, como abordaje macroeconómico, se plantea como la única salida viable y sostenible al actual sistema de producción basado en el consumo de combustibles fósiles.
Durante el desarrollo de la primera Revolución Industrial quedó claro que el empleo de madera (fuente renovable, limitada por la deforestación) no iba a ser suficiente para cubrir los requerimientos energéticos demandados por la industria.
Ante esta situación, el desarrollo tecnológico optó por la utilización de combustibles fósiles (fuentes no renovables, dependientes de reservas) como el carbón y el petróleo. Décadas de convivencia con estas materias primas han generado una economía global fuertemente dependiente, ligando su viabilidad únicamente a la disponibilidad de petróleo.
Esta escasa resiliencia genera un modelo productivo insostenible a medio-largo plazo al estar económicamente afectado por la disponibilidad de una materia prima no renovable (susceptible a cambios bruscos en su valor de mercado) y medioambientalmente nociva debido a las emisiones de CO2 en su combustión.
Con todo lo mencionado, la única manera de generar una economía global viable a largo plazo pasa por sustituir la «economía del petróleo» por la «bioeconomía»
Este nuevo sistema será el encargado de sostener en un futuro la industria química y de combustibles, actualmente copada por los combustibles fósiles, mediante el empleo de fuentes renovables de origen biológico.
La investigación y desarrollo (I+D) que en su día propició la eficiente implementación de una industria basada en el petróleo, ha dado lugar a un gran progreso en los campos de la ingeniería y la química. Sin embargo, estas ramas de conocimiento van a necesitar ser fuertemente complementadas para el desarrollo de la mencionada bioeconomía.
En este punto, la biología sintética se posiciona como un pilar fundamental para tal propósito. De hecho, el abandono del petróleo como la materia prima fundamental para procesos químicos es uno de los pilares de la así llamada «Cuarta Revolución Industrial», que pone el énfasis en la economía circular (cero residuos) y la deslocalización y automatización de todas las cadenas de producción.
Biología sintética: el combustible necesario para el progreso de la bioeconomía
La bioeconomía, por definición, se encuentra íntimamente ligada al desarrollo biotecnológico. A su vez, la biotecnología está sufriendo una importante revolución, liderada por la aparición de un nuevo campo denominado biología sintética. Esta disciplina emerge gracias a la convergencia, de la ingeniería, de las diferentes biociencias y las tecnologías de la información.
En las últimas décadas se ha generado un enorme conocimiento biológico que ha venido acompañado de una acumulación de gran cantidad de datos. El mayor ejemplo está encabezado por las denominadas «ómicas», que integran disciplinas como la genómica o la proteómica, encargadas de estudiar en su totalidad las funciones e interacciones comprendidas por los genes y proteínas de un organismo.
Este tipo de tecnologías vienen acompañadas de la generación de una gran cantidad de información que, en última instancia, han permitido desentrañar la complejidad biológica de multitud de sistemas vivos, llegando a comprender cómo funcionan cada una de las partes que los componen (genes, proteínas).
De esta manera ha sido posible establecer una analogía entre un sistema vivo (por ejemplo, una bacteria o una célula eucariota) y una máquina, comprendiendo su funcionamiento mediante el conocimiento de los elementos que la componen (proteínas vs. engranajes).
La biología sintética surge entonces como una evolución de la clásica ingeniería genética, abandonando el enfoque tradicional de experimentación mediante «ensayo y error», de cara a adoptar el punto de vista de la ingeniería. El conocimiento funcional de la maquinaria celular permite a la biología sintética la ingeniería de sistemas biológicos complejos con nuevas funciones, todo ello desde una perspectiva racional y sistemática. En otras palabras, al igual que se aplicaría en la construcción de un automóvil, la biología sintética permite mediante el conocimiento de las partes el diseño de un sistema biológico con un fin determinado. A su vez, esta rama de la biología persigue la caracterización de estos elementos biológicos, permitiendo su estandarización como si de tornillos de una maquinaria se tratase.
Este abordaje de diseño racional es especialmente atractivo de cara a obtener un determinado producto de interés, situando a la biología sintética como una herramienta clave en multitud de sectores enmarcados en la bioeconomía.
Dando forma a la bioeconomía desde la I+D en biología sintética
El apoyo económico institucional como clave para el desarrollo del binomio biología sintética-bioeconomía
La posición privilegiada que ocupa la biología sintética dentro del marco de la bioeconomía ha quedado reflejada en multitud de programas institucionales de financiación. La Unión Europea (UE) ha demostrado en los últimos años su marcado compromiso a la hora de fomentar la I+D involucrada directamente en la estrategia bioeconómica. Dicho camino comenzó con la convocatoria Cell Factory dentro del 5.º Programa Marco (1998-2002), llegando a nuestros días con la creación de la «Estrategia Europea en Bioeconomía» (2012) ampliamente recogida en la hoja de ruta del Programa Horizonte 2020 (2014-2020).
Todo este esfuerzo por parte de la UE se ha visto acompañado desde otras partes del planeta, siendo un ejemplo notable el papel jugado por los Estados Unidos de América (EEUU) donde en 2006 fue creado con carácter innovador el Synthetic Biology Engineering Research Center (SynBERC), ahora conocido como Engineering Biology Research Consortium (EBRC), un centro de investigación multidisciplinar focalizado en la comercialización de productos derivados de la actividad de la biología sintética –National Academy of Engineering and National Research Council–.
Acelerando los procesos de I+D en búsqueda de una bioeconomía más competitiva
Las iniciativas de financiación como las anteriormente citadas están permitiendo a la biología sintética el desarrollo y perfeccionamiento de tecnologías fundamentales para la investigación pública e industrial, tales como:
- Secuenciación de ADN. La biología sintética, desde su perspectiva de ingeniería siempre ha tomado como pilar básico el conocimiento de la secuencia exacta de nucleótidos que componen los diferentes elementos genéticos bajo estudio (p. ej.: cromosomas). En la actualidad, la secuenciación de ADN se presenta como un claro ejemplo en cuanto a la democratización de las técnicas de biología molecular se refiere. Lejos quedan los tiempos en que un proyecto de secuenciación de ADN, como por ejemplo la secuenciación del genoma humano (2004), solo era posible gracias a la colaboración económica y la unión de esfuerzos entre diferentes instituciones. El desarrollo de nuevas técnicas como la secuenciación de última generación (Next-Generation Sequencing, NGS) y la aún más novedosa secuenciación de tercera generación (Third-Generation Sequencing) han permitido un abaratamiento en costes y esfuerzos sin precedente en la industria. Para ser más precisos, la aplicación de estas nuevas tecnologías ha supuesto a día de hoy un abaratamiento en costes de unas 10.000 veces en comparación con el desempeñado durante la secuenciación del genoma humano en 2004. El abaratamiento en la secuenciación de ADN aumenta la accesibilidad de esta técnica a diferentes niveles, acelerando los procesos de I+D y permitiendo a la industria la incorporación de dichas técnicas en sus sistemas de producción y control de calidad.
- Síntesis y ensamblado de ADN. Las ya citadas «ómicas» han permitido delimitar las funciones de diferentes elementos biológicos dentro de las células. Por ejemplo, es posible concretar el número de genes necesarios para completar la síntesis de un determinado producto por parte de una bacteria. Las técnicas clásicas de biología molecular permitían el intercambio de dichos genes entre diferentes organismos mediante un simple método de «copia y pega». Sin embargo, en la actualidad ya no es necesario recurrir a este abordaje, siendo posible sintetizar «a la carta» la secuencia de ADN que contenga los genes de interés, y modificarla a nuestro antojo según deseemos. Durante la presente década la síntesis de novo de ADN ha sufrido un enorme avance en lo que a fidelidad y coste se refiere. La implementación de la síntesis de ADN basada en microchips ha permitido a la industria la miniaturización y automatización del proceso. Siguiendo este camino, es posible sintetizar en la actualidad fragmentos de ADN con un tamaño considerable de nucleótidos, de gran fidelidad y con un coste 100 veces inferior al encontrado en las primeras fases de desarrollo de la técnica. Por si fuera poco, el desarrollo de técnicas automatizadas robustas de ensamblaje de ADN in vitro permite, mediante la unión de estos fragmentos, la producción de cadenas con más de 2.000 pares de bases de longitud. Ejemplo de todo ello es la posibilidad de sintetizar a día de hoy, y de forma completa, el cromosoma de diferentes microorganismos (p. ej.: levaduras y bacterias). Tales avances permiten a la I+D e industria verse únicamente limitados por el conocimiento presente hasta la fecha, y no por la metodología y el coste, pudiendo optar por sintetizar a voluntad el ADN necesario de cara a mejorar los procesos deseados.
- Herramientas de manipulación genética. El alto grado de conocimiento alcanzado a la hora de asociar gen y función hace posible focalizar el diseño experimental hacia determinadas modificaciones de la secuencia de ADN. Una de las ramas más potentes en biología sintética ha sido la encargada de desarrollar metodologías que faciliten la manipulación del ADN de forma precisa y controlada, deleccionando, insertando o modificando la secuencia de nucleótidos a nuestro antojo. El año 2013 marcó un antes y un después en lo que a edición genética se refiere, dándose a conocer el enorme potencial de la tecnología CRISPR/Cas9. Descubierto como un sistema de defensa contra la infección de virus en bacterias, el sistema CRISPR/Cas9 ha sido adaptado como un sistema eficaz y preciso de manipulación genética, demostrando su utilidad en multitud de organismos, incluyendo al ser humano. Su bajo coste y simplicidad han revolucionado la era de la ingeniería genética, haciendo accesible a la I+D e industria la manipulación precisa del ADN de sus organismos de interés.
- Modelado in silico de sistemas biológicos complejos. El desarrollo de modelos matemáticos predictivos robustos se presenta como una potente herramienta en el campo de la biología sintética. El modelado in silico de determinadas funciones celulares, como rutas metabólicas o circuitos genéticos, permiten el diseño racional de complejos sistemas biológicos. La capacidad de poder predecir informáticamente determinadas funciones biológicas supone un gran adelanto en términos de economía experimental, reduciéndose en coste y tiempo el trabajo necesario en el laboratorio. Este abordaje supone una aceleración en los ciclos de I+D, permitiendo a su vez a la industria nutrirse de una forma más rápida de los diferentes avances científicos, haciendo más competitivo el sector bioeconómico.
Apoyándose en estos avances tecnológicos clave, la biología sintética tiene el potencial de revolucionar los ciclos de producción biotecnológicos (Figura 1). Al igual que otras industrias, la biotecnológica depende de una fuerte interconexión entre sus diferentes etapas de desarrollo. El fin último de todo proceso industrial pasa por la entrega al consumidor de un producto, y para llegar a la obtención de este, es necesaria la consecución exitosa de una fase de investigación y producción. Esta última, especialmente en el caso de la industria biotecnológica, presenta dos actores principales: la clásica industria biotecnológica y las emergentes industrias start-up (industrias emergentes).
Estas industrias start-up buscan escapar del encorsetado tejido clásico de producción. Focalizan su negocio en sectores innovadores, de carácter creativo (y por tanto diferencial), que persiguen simplificar procesos más complejos de la industria clásica manejando un capital de riesgo elevado. Esta filosofía ha resultado de gran atractivo en diferentes procesos relacionados con la biología sintética, generando una marcada innovación, de la cual se han nutrido tanto los procesos de investigación como aquellos de producción más clásicos.
En resumen, la biología sintética está transformando los clásicos ciclos de producción biotecnológicos, implementando una serie de métodos destinados a mejorar los costes, velocidad y viabilidad de sus procesos (Figura 1):
- El modelado in silico ha permitido reducir los experimentos de «ensayo y error» considerados como abordaje básico con anterioridad. Su optimización ha permitido la reducción en los tiempos de I+D, permitiendo a la par evaluar la viabilidad de proyectos que debido a su alto riesgo podrían ser descartados en una industria biotecnológica más clásica y conservadora.
- La perspectiva de ingeniería que guía a la biología sintética tiene como premisa la caracterización de los elementos funcionales que la componen (p. ej. los genes). A su vez, se persigue el tratamiento de estos como elementos estandarizados, tendiéndose a la unificación de los mismos en diseño, nomenclatura y descripción. Dicho sistema permite la creación de grandes colecciones de componentes genéticos estandarizados, que facilitan su intercambio, posibilitando la reutilización y optimización de estos para diferentes propósitos. Este ambiente de trabajo repercute en una importante aceleración de los procesos de I+D, facilitando las estrategias a seguir en las industrias de producción al tratarse de componentes genéticos bien caracterizados.
- La aparición de numerosas empresas biotecnológicas especializadas, en muchos casos de tipo start-up o spin-off, ha permitido desvincular a la I+D de diferentes procesos de manufactura, como la síntesis y secuenciación de ADN (DNA-Script, 2017 y CIBCSIC, 2018). Este desacoplamiento de funciones ha permitido la creación de nuevas empresas con un importante nicho de negocio, a la par que la investigación puede centrarse exclusivamente en la innovación y no en la producción.
- El proceso de estandarización perseguido por la biología sintética hace a esta disciplina susceptible de automatización y escalado. El resultado de este diseño repercute en una importante reducción de los ciclos de I+D, facilitando al mismo tiempo el escalado de sus resultados a un mayor volumen de producción industrial.
Con todo ello, es posible dibujar multitud de sinergias entre la biología sintética y los diferentes elementos de la industria biotecnológica, entendiendo esta como uno de los principales pilares de la bioeconomía (Figura 1). Al contrario de lo que cabría esperar, el desarrollo de la biología sintética no se centra única y exclusivamente en la aceleración de los procesos de I+D, sino que potencia a su vez los elementos productivos y por consiguiente el resultado que llega al consumidor.
Figura 1. Sinergias entre el espacio de la biología sintética y el tejido productivo bioeconómico
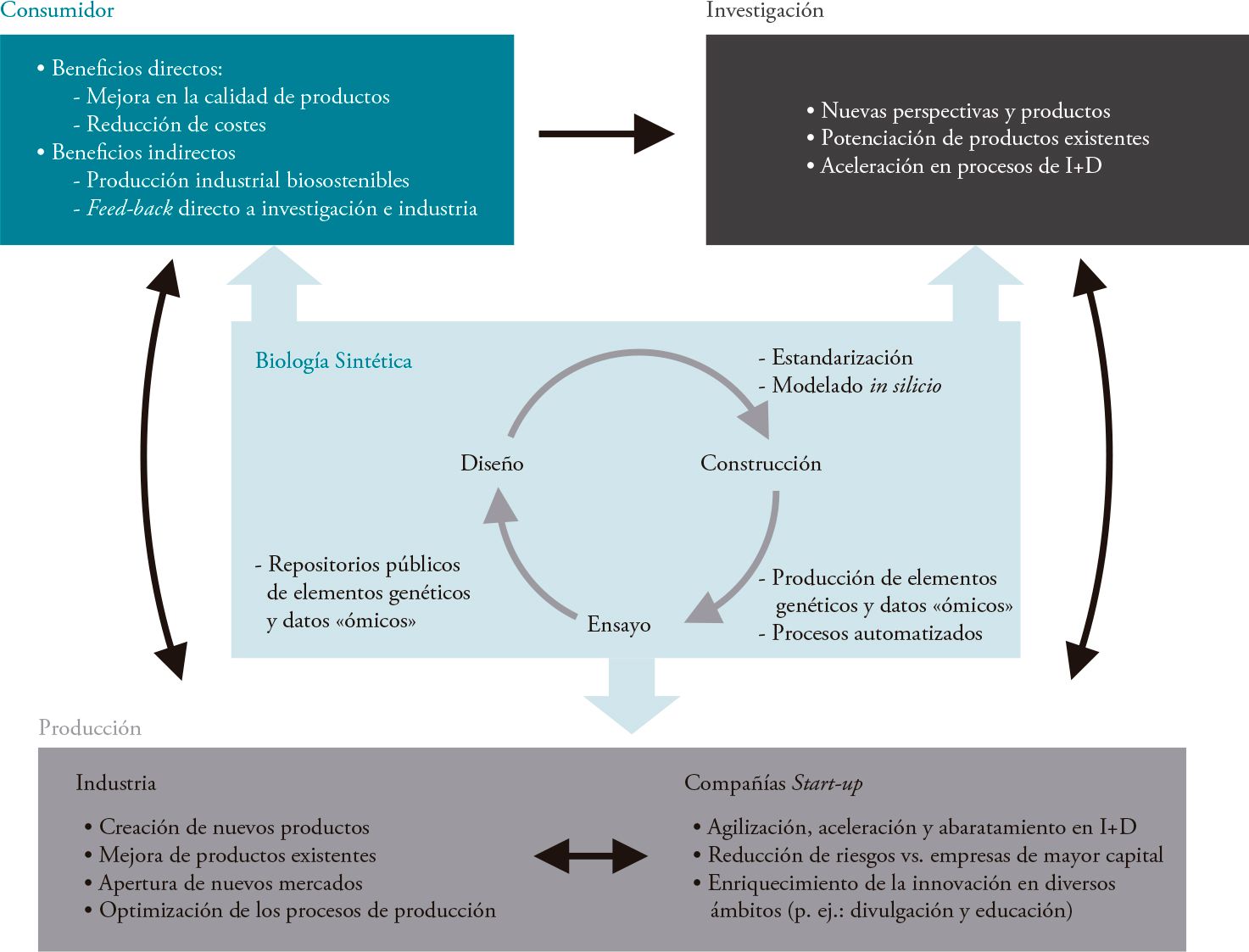
El ciclo de producción biotecnológico se encuentra íntimamente interconectado. Las flechas dispuestas a lo largo de esta figura designan el flujo de influencia existente entre los diferentes sectores del mercado biotecnológico. Cada caja coloreada comprende un diferente sector, enumerándose en cada uno de ellos las características que les otorga relevancia. En el centro de la imagen aparece reflejada la biología sintética y su propio ciclo de desarrollo (diseño-construcción-ensayo), describiéndose los hitos que han resultado relevantes en el desarrollo de la industria biotecnológica.
¿De qué es capaz la biología sintética? Reformulando la industria tradicional basada en el petróleo
Si la bioeconomía pretende sustituir a la industria tradicional basada en el petróleo, esta debe asumir totalmente sus competencias. En la actualidad, el petróleo se sitúa como una fuente esencial a la hora de conseguir combustible, químicos y materiales. La bioeconomía, mediante un enfoque basado en biología sintética de vanguardia, persigue obtener todos esos bienes partiendo de fuentes biológicas renovables. Si bien este último enfoque no se ha implementado aún de forma global, a continuación, se muestra cómo el campo de la biología sintética está afrontando el desafío de desterrar la dependencia del petróleo en dos campos clave: la producción de combustibles y la creación de compuestos plásticos.
Los biocombustibles como solución a largo plazo
El petróleo es una fuente de energía poderosa a la par que limitada, localizada y no renovable. Las reservas de esta materia prima son cada vez más escasas y de peor calidad, lo que encarece su utilización de forma continuada. La mayoría de la maquinaria que nos rodea emplea derivados de este combustible fósil para operar, como son el queroseno en aeronáutica, o la gasolina y el diésel en automoción. Reconvertir todo este aparataje para emplear otra fuente de energía alternativa supondría un esfuerzo insostenible. La solución a esta problemática pasa por la creación de combustibles capaces de trabajar en esta maquinaría ligeramente adaptada, con la salvedad, de obtenerse a partir de fuentes de energía biológicas renovables.
La historia de los biocombustibles es larga, siendo el bioetanol y biodiésel los más empleados y desarrollados hasta la fecha. En ambos se parte de materia vegetal para su manufactura, siendo en la mayoría de los casos cultivos destinados ex profeso para tal fin. Dicha realidad ha suscitado en la opinión pública la controversia entre el cultivo alimentario vs. el cultivo para biocombustibles, acrecentada por las numerosas hambrunas desarrolladas en los últimos años (Somalia, 2011 y Sudán del Sur, 2017). Junto al componente ético-social se presenta la gran dificultad técnica para obtener estos biocombustibles, necesitando para ello de complejas fermentaciones y tratamientos químicos. Así, la utilización de estos biocombustibles no se plantea como algo opcional, sino como una obligatoriedad, especialmente si tenemos en cuenta la proyección a largo plazo del petróleo.
Como cabría esperar, la biología sintética tiene algo que aportar al respecto, añadiendo una perspectiva diferente a la producción de biocombustibles. Un ejemplo extraordinario de esta táctica es el trabajo publicado por Bokinsky y colaboradores, en el que se describe como la bacteria Escherichia coli se modificó genéticamente con el fin de producir precursores para la síntesis de gasolina, gasoil y queroseno. Este trabajo presenta a esta bacteria como una biorrefinería viviente que es capaz de expresar por sí sola todos los elementos necesarios para transformar materia vegetal en biocombustibles, sin necesidad de llevar a cabo complejos procesos de purificación y fermentación (Figura 2a).
La celulosa es un biopolímero compuesto exclusivamente por moléculas de glucosa, y a su vez, es la biomolécula con más presencia en la Tierra, al ser el componente esencial de las paredes vegetales. Este microorganismo, gracias a su manipulación genética, es capaz de expresar las enzimas necesarias para degradar esta celulosa en azúcares libres (unidades de glucosa). A su vez, la ingeniería genética realizada sobre E. coli le permite emplear estos azúcares para crecer y producir los precursores de biocombustibles. Este abordaje permite acumular en una misma célula lo que en la actualidad reúne una completa biorrefinería: degradación de biomasa y producción de biocombustibles.
Ejemplos como el anterior demuestran el gran potencial que tiene la biología sintética en el campo de la producción de biocombustibles y, por ende, en la bioeconomía. Todos estos abordajes se encuentran aún en fase de experimentación, pero una vez superen las limitaciones propias de la innovación, serán una fuerte herramienta para olvidar nuestra dependencia hacia los combustibles fósiles.
Bioplásticos, y biopolímeros generados mediante biología sintética
La presencia de plásticos en nuestra vida cotidiana se hace más que patente cuando miramos a nuestro alrededor. La mayoría de estos compuestos son producidos a partir del petróleo, con las problemáticas asociadas ya mencionadas. Por si esto no fuera suficiente, su tasa de degradación es ínfima, acumulándose en el medioambiente con unas consecuencias nefastas. Así pues, la sustitución de la industria plástica tradicional por una de bioplásticos de origen biológico y biodegradables se muestra como un asunto capital de cara a garantizar su presencia y sostenibilidad.
Al igual que en el caso de los biocombustibles, la producción de bioplásticos en la actualidad se encuentra soportada por fuentes de origen vegetal (p. ej.: almidón de maíz). En el caso de los bioplásticos provenientes del ácido poliláctico o PLA, su producción se basa en la fermentación de biomasa vegetal para obtener ácido poliláctico. Este monómero se polimeriza y purifica posteriormente mediante complejos procesos que envuelven altas temperaturas, disolventes y metales pesados. De nuevo, la biología sintética se plantea como una herramienta para facilitar procesos como los mencionados anteriormente. Por ejemplo, ya se han generado bacterias de la especie E. coli cuyo metabolismo se ha redirigido y modificado para producir PLA a partir de glucosa de forma eficiente, evitando complejos tratamientos de polimerizado y purificación (Figura 2b).
Figura 2. Microorganismos como biofactorías
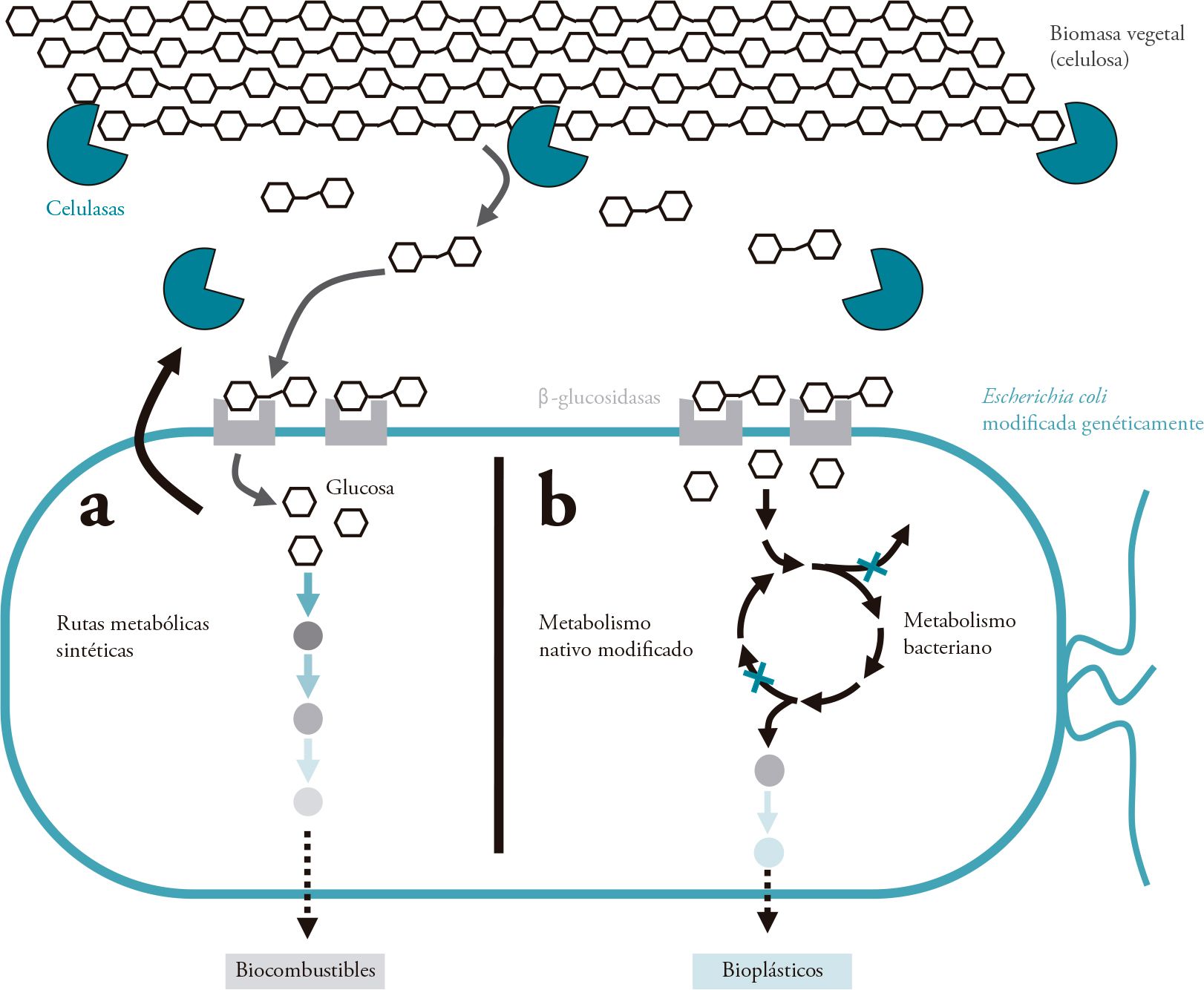
La imagen ejemplifica los diseños que la biología sintética ha explorado para la generación de biocombustibles y bioplásticos. Las bacterias modificadas genéticamente producen enzimas celulasas (señaladas en verde) y β-glucosidasas (señaladas en gris) que permiten descomponer la celulosa que compone la biomasa vegetal en unidades de glucosa. a) La introducción de rutas metabólicas sintéticas permite transformar la glucosa en diferentes precursores de biocombustibles. b) La modificación del metabolismo nativo de la propia bacteria (p. ej.: eliminando actividades mediante delección de genes metabólicos), junto con la introducción de genes productores de biopolímeros, permite canalizar los intermediarios del metabolismo de glucosa con el fin de incrementar la producción de bioplásticos.
Los bioplásticos PLA son una interesante alternativa en el mercado, pero tal y como ocurre con los plásticos provenientes del petróleo, la existencia de otros bioplásticos con diferentes propiedades (p. ej.: elasticidad y resistencia) se hace necesaria en una futura bioconversión de la industria. La biología sintética también ayuda a dar respuesta a esta demanda, centrando sus esfuerzos en la producción de bioplásticos como los polihidroxialcanoatos o PHA. Estos poliésteres lineales son producidos en la naturaleza mediante la fermentación de azúcares y lípidos por parte de bacterias. Los microorganismos acumulan estos polímeros en su interior con la intención de obtener una reserva de carbono para periodos de escasez, siendo uno de sus grandes exponentes la especie Cupriavidus necator.
Diferentes grupos de investigación, haciendo uso de biología sintética, están tomando como inspiración los genes de producción de PHA que se encuentran en bacterias como C. necator y Pseudomonas putida. Haciendo uso de esta información genética es posible modificar bacterias más manejables industrialmente como E. coli, consiguiendo microorganismos biofactoría con una importante producción de bioplásticos tipo PHA. Estos polímeros se pueden incluso funcionalizar biológicamente para dotar a los materiales resultantes de propiedades más allá de sus meras características físicas.
Biología sintética, bioeconomía y sociedad
Por último, y no menos importante, es necesario remarcar la trascendencia que tiene la comunicación entre todas las partes interesadas en el desarrollo de la bioeconomía. Los científicos no pueden obviar la repercusión que sus trabajos tienen en la sociedad, siendo de vital importancia la correcta difusión de sus resultados ante la opinión pública y los organismos reguladores. Un entorno de correcta comunicación y divulgación, entendiéndolo siempre desde un enfoque bidireccional entre ciencia y sociedad, es la única opción para desarrollar todo el potencial que la biología sintética puede ofrecer para el desarrollo bioeconómico.
Regulación y bioseguridad
En la actualidad, la mayoría de expertos consideran que las regulaciones legales y la proyección de riesgos en lo relativo a la biología sintética pueden ser cubiertos por los ya existentes en materia de ingeniería genética. A medio plazo, se asume que el empleo de biología sintética no supone un riesgo ni genera nuevas cuestiones en lo que a bioseguridad se refiere. No obstante, es necesario una constante vigilancia y una evaluación de leyes en consonancia con los avances científicos.
En términos de bioseguridad, se debe hacer hincapié en la dicotomía que este término presenta en castellano (biosafety vs. biosecurity). Entendiendo bioseguridad como biosafety en inglés, se hace referencia a la serie de políticas y prácticas desarrolladas con el fin de proteger al trabajador y medioambiente de sucesos fortuitos y accidentales. En este caso la principal problemática es la falta de una apropiada formación, junto a una correcta concienciación, que resalte lo crítico de trabajar en un ambiente de laboratorio. Estas cuestiones son especialmente importantes en un entorno multidisciplinar como en el que se desarrolla la biología sintética, siendo necesaria una mayor atención en términos de bioseguridad para aquellos profesionales más ajenos al trabajo en laboratorio con organismos vivos (p. ej.: ingenieros computacionales o químicos sintéticos).
Por otro lado, el término bioseguridad como biosecurity en inglés, hace referencia al control del material biológico e información para obtener este con el fin de prevenir una posesión indebida y/o un uso malintencionado (p. ej.: liberando agentes vivos al medioambiente). En lo que respecta a la normativa de la UE, se asume que la regulación actual en términos de bioseguridad es suficiente para afrontar los desafíos emergentes del uso de la biología sintética. Al tratarse de una disciplina de vanguardia, es necesario a su vez realizar un seguimiento cercano de sus actividades y productos, siendo relevante el papel que en la UE desarrolla el Scientific Committee on Emerging and Newly Identified Health Risks (SCENIHR 2015). Esta institución aconseja una serie de medidas de cara a garantizar una continua seguridad y protección en cuanto a bioseguridad se refiere, haciendo a la vez especial hincapié en la proporcionalidad de estas, a fin de no comprometer la seguridad ni tampoco el dinamismo investigador.
El SCENIHR propuso en 2015 como puntos de partida para una biología sintética segura: (i) caracterizar detalladamente los elementos biológicos en estudio a la par que del desarrollo de herramientas computacionales para predecir las propiedades emergentes de los mismos; (ii) optimizar y estandarizar los métodos de comunicación con los agentes asesores de riesgos en materia de modificaciones y herramientas genéticas; (iii) incentivar al uso de organismos modificados genéticamente (OMG) cuya funcionalidad y seguridad hayan sido contrastadas; (iv) asegurarse que los métodos de evaluación de riesgos y los avances en biología sintética evolucionan de forma paralela; y (v) apoyar el intercambio de información relevante sobre elementos, dispositivos y sistemas biológicos con los agentes asesores de riesgo. El cumplimiento de estas directrices, asumiendo la organización estandarizada que deben cumplir los elementos biológicos generados mediante biología sintética, asegura un entorno de bioseguridad que no sacrifica el progreso.
A fin de concluir este apartado que atañe a la bioseguridad, no debemos olvidar cómo el desarrollo de la biología sintética ha permitido la democratización de multitud de técnicas moleculares. El ya mencionado abaratamiento y accesibilidad que han sufrido técnicas como la secuenciación, síntesis y manipulación de ADN generan un escenario novedoso en el cual ya no es necesaria la posesión de un laboratorio sofisticado para realizar biología sintética. Esto puede presentarse como una extraordinaria situación de cara a hacer más accesible la ciencia a la sociedad, pero a la par facilita el empleo malicioso de estas técnicas. Teniendo en cuenta todo ello, expertos como Schmidt y Giersch sostienen que deben supervisarse aspectos como: (i) controlar la difusión de secuencias de ADN que permitan la síntesis de cromosomas y toxinas procedentes de conocidos patógenos; (ii) hacer un control de los clientes de tecnologías de síntesis de ADN para evitar usos inapropiados; y (iii) controlar la distribución de equipamiento y sustancias necesarias para la síntesis de oligonucleótidos.
Los lazos entre sociedad y biología sintética: normalizar la bioeconomía
Pocas dudas quedan sobre el beneficioso papel que debe adquirir la bioeconomía a la hora de combatir los grandes retos a nivel global que se plantean. A su vez, ha quedado claro el enorme potencial que presenta la biología sintética como plataforma tecnológica en el desarrollo de la bioeconomía. Sin embargo, existe una gran problemática en cuanto a la reacción adversa que presenta una gran parte de la sociedad frente a la utilización de la tecnología de OMG, especialmente en la UE. Esta confrontación puede impactar negativamente en el desarrollo de la biología sintética y, por ende, ralentizar la aplicación de una potente bioeconomía.
Teniendo en cuenta todo lo mencionado, debe ser prioritario en las agendas de las diferentes instituciones públicas de investigación la creación de proyectos multidisciplinares que faciliten el intercambio de opiniones ciencia-sociedad. Profesionales de la investigación con amplios conocimientos en divulgación se muestran clave de dicha estrategia. A su vez, no debe olvidarse la demanda de profesionales que la biología sintética requerirá en un futuro, siendo la educación de los jóvenes un objetivo prioritario. Competiciones de biología sintética como el iGEM (www.igem.org), en el que diferentes equipos de estudiantes se enfrentan para desarrollar un proyecto científico corto e innovador, acerca a los más jóvenes a esta disciplina a la par que se refuerza el dialogo con la opinión pública.
Por último, debe destacarse el enorme grado de expansión que está alcanzando la biotecnología gracias a la biología sintética, permitiendo a esta última introducirse en industrias hasta entonces ajenas a su actividad. Un gran ejemplo de esta exótica expansión es la creación de start-up que aúnan en un mismo proyecto los conceptos «fácil de usar», «biología sintética» y «hazlo tú mismo en casa». Proyectos como Amino Labs (www.amino.bio) y Bento Labs (www.bento.bio) han desarrollado sencillos kits con los que realizar sencillos experimentos de biología sintética desde la propia casa, suponiendo una novedosa fuente de negocio a la par que educativa y divulgativa.
Conclusiones
Durante el desarrollo del presente capítulo ha sido posible demostrar la estrecha relación existente entre la biología sintética y la bioeconomía. Desde un punto de vista holístico, es posible definir la relación de ambos términos como una sinergia en expansión. El desarrollo de la bioeconomía se encuentra estrechamente relacionado al sector biotecnológico. Dicho sector ha sido impulsado en la actualidad gracias al enfoque tomado de la ingeniería y adoptado por la biología Sintética, que sirve finalmente como la herramienta tecnológica idónea para la evolución de la bioeconomía.
La innovación que define a la biología sintética como campo de investigación ha permitido el desarrollo de multitud de técnicas que han revolucionado las ciencias moleculares. Unido a estos avances, encontramos el cambio de filosofía que ha supuesto la biología sintética para las biociencias, definiendo a los organismos vivos como máquinas cuyas partes (o piezas) puede ser entendidas, estandarizadas y reutilizadas con el fin de obtener un beneficio concreto. Todo ello ha permitido que la biología sintética potencie directamente todos los sectores del tejido productivo biotecnológico, desde el consumidor al productor, evitando ceñirse en exclusiva a la previsible I+D.
La bioeconomía se cimienta en la utilización de fuentes biológicas renovables como pilar fundamental de la industria del futuro. Es la única salida viable a la dependencia nociva que presenta el uso del petróleo y sus derivados. Ejemplos como los citados para la producción de biocombustibles y bioplásticos definen a la biología sintética como una herramienta primordial en la implementación de una bioeconomía real.
Un cambio tan profundo a nivel global como el perseguido por la bioeconomía no puede prescindir de un enfoque social responsable. Sus herramientas esenciales, como la biología sintética, deben contar con una vigilancia adecuada y proporcionada en materia de bioseguridad. Está supervisión debe realizarse garantizando en todo momento la protección social, sin por ello limitar o penalizar los avances científicos. Encontrar el balance perfecto entre riesgo e innovación dependerá en gran medida del éxito en políticas de educación y divulgación, siendo estas últimas un elemento clave a la hora de hacer a la sociedad participe del éxito y desarrollo de la estrategia en bioeconomía.


